眾所周知,藥品注冊資料涉及安全性、藥學、臨床等方面的內容,作為專業的醫學翻譯,譯員首先要了解注冊申報資料中常用的詞匯和語言表達習慣;其次,了解藥品注冊法規和熟悉藥典也是非常有必要的。在全套藥品注冊資料中,CMC 藥學資料是新藥申報中非常重要的模塊,包括原料藥模塊,制劑模塊,輔料的控制等內容。
今天,康茂峰醫學翻譯跟大家分享一下中國藥典中對輔料凝膠劑(Gel)的介紹。
凝膠劑(Gel)是指藥物與能形成凝膠的輔料制成均一、混懸或乳狀液形的稠厚液體或半固體制劑。能形成凝膠的輔料有泊洛沙姆(Poloxamer)、依地酸二鈉(EDTA Disodium)、多庫酯鈉(Docusate sodium)、丙二醇(Propylene glycol)。像我們常見的凝膠藥品有甲硝唑凝膠(Metronidazole Gel)、他扎羅汀凝膠(Tazarotene Gel)、對乙酰氨基酚凝膠(Paracetamol Gel)、異維A 酸凝膠(lsotretinoin Gel)、過氧苯甲酰凝膠(Benzoyl Peroxide Gel)等等。
中國藥典2020年版第四部通則0114凝膠劑中對凝膠劑的生產與貯藏期間有以下規定:
一、膠劑中膠粒應分散均勻,不應下沉、結塊。
二、凝膠劑應均勻、細膩,在常溫時保持膠狀,不干涸或液化。
三、根據需要,凝膠劑中可加人保濕劑、抑菌劑、抗氧劑、乳化劑、增稠劑和透皮促進劑等。除另有規定外,在制劑確定處方時,該處方的抑菌效力應符合抑菌效力檢查法(通則1121)的規定。
四、凝膠劑一般應檢查pH值。
五、除另有規定外,凝膠劑應避光、密閉貯存,并應防凍。
六、凝膠劑作為無菌制劑時,應進行無菌檢查;作為非無菌制劑時,應進行非無菌檢查。
除另有規定外,凝膠劑還應進行以下相應檢查。
粒度:檢查法為取供試品適量,置于載玻片上,涂成薄層,薄層面積相當于蓋玻片面積,共涂3片,照粒度和粒度分布測定法(通則0982第一法)測定,均不得檢出大于180 μm的粒子。
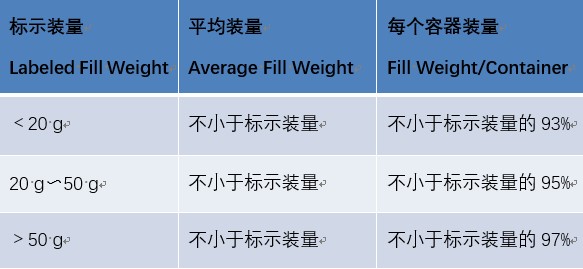
裝量:照最低裝量檢查法(通則0942)檢查,可采用重量法(適用于標示裝量以重量計的制劑),除另有規定外,取供試品5個(50 g以上者3個),除去外蓋和標簽,容器外壁用適宜的方法清潔并干燥,精密稱定重量,除去內容物,容器用適宜的溶劑洗凈并干燥,再精密稱定空容器的重量,求出每個容器內容物的裝量與平均裝量,均應符合下表的有關規定。如有1個容器裝量不符合規定,則另取5個(50 g以上者3個)復試,應全部符合規定。